检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
RNA碱基编辑作为一项全新的疾病治疗策略,越来越受到广泛关注。ADAR作为一种细胞内源的RNA脱氨酶已经被广泛应用于RNA碱基编辑。基于ADAR的RNA编辑利用了细胞翻译机制的一个独特性质,即由于结构相似性,肌苷会被识别为鸟嘌呤。这使得ADAR编辑器能够引入特定位点的、由RNA引导的腺嘌呤到肌苷(A-to-I)的改变,从而打开了广泛的治疗潜力,包括修正致病突变、调节基因表达或改变蛋白质相互作用等[1]。2019年魏文胜课题组开发了LEAPER技术(Leveraging Endogenous ADAR for Programmable Editing of RNA) [2],并于2022年升级为LEAPER 2.0 [3],通过工程化的环状RNA招募细胞内源的ADAR蛋白,在靶向位点实现了高效且精准的编辑。由于LEAPER是一种依赖于内源ADAR活性的编辑系统,而不同组织和物种中内源 ADAR 的表达存在差异,并且递送方法尚未得到全面验证,因此该技术仍需在多个物种,特别是非人灵长类中进行测试。在这项研究中,研究人员进一步利用AAV将工程化的环状ADAR招募RNA(circ-arRNA)递送到非人灵长类动物及人源化小鼠体内,以实现长期、高效和精准的RNA碱基编辑。
首先,研究人员在非人灵长类动物的体外培养细胞内进行了实验,通过优化获得了高效且精准的工程化circ-arRNA,其靶向位点的编辑效率可高达47%。随后,他们将该工程化circ-arRNA包装到AAV病毒中,成功实现了在非人灵长类动物体内的递送。然而,临床上使用的AAV剂量一旦超过1 × 1014 vg/kg,会带来严重毒性[4],因此该研究将AAV剂量控制在临床可接受的范围内,分别为3×1012,1×1013和3×1013 vg/kg的剂量 (图1A)。将这三种剂量的肝靶向AAV8注射到非人灵长类动物体内,并进行长期观察和检测,结果显示在第二周,肝脏细胞编辑效率可达50%以上(图1B)。通过计算感染效率(图1C)发现受AAV感染的肝脏细胞编辑效率可高达80%,这表明LEAPER 2.0可以在体内快速且高效地发挥作用。此外,研究人员还发现,编辑效率呈剂量依赖性,随着AAV8剂量的升高,非人灵长类动物体内工程化circ-arRNA的表达量增加,从而提高了编辑效率,这表明LEAPER 2.0具有良好的药物剂量依赖性 (图1D)。编辑效率在非人灵长类动物体内可以维持13周并保持稳定,说明通过AAV递送的LEAPER 2.0具有长期编辑的特点(图1E)。此外,研究者未观察到LEAPER 对非人灵长类动物具有毒性,表明该编辑技术是安全且特异的。
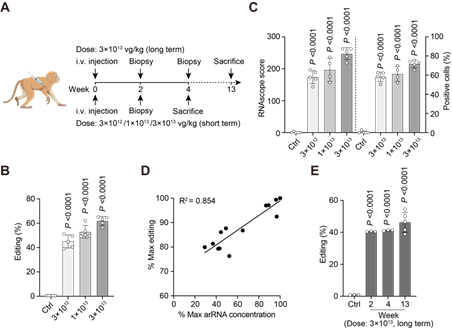
图1. AAV递送的LEAPER 2.0在非人灵长类动物体内实现高效、长时程编辑
进一步地,研究人员尝试使用AAV递送的LEAPER 2.0来治疗人源化转录本中的提前终止密码子。提前终止密码子导致了11%的人类遗传病[5],因此针对此类密码子的编辑具有巨大的应用前景。为此研究者构建了人源化的Hurler综合征小鼠,该小鼠表达人源化的IDUA转录本,其中存在一个提前终止密码子,导致该小鼠可以模拟人类溶酶体贮积症,即粘多糖贮积症 I 型 (MPS-I)(图2A)。 MPS-I的特征是α-L-艾杜糖苷酶的酶活性缺陷,导致糖胺聚糖 (GAG)的积累。通过筛选和理性设计,研究者成功地提高了ADAR编辑的精确性,并获得了高效的工程化circ-arRNA。使用AAV-PHP.eB递送circ-arRNA到小鼠体内,不仅在肝脏等器官,而且在神经系统恢复了α-L-艾杜糖苷酶的酶活性(图2B,C),降低了GAG的积累,显著改善了小鼠的表型。由于目前MPS-I的治疗策略多为酶替代疗法,递送的IDUA蛋白不能跨越血脑屏障,因此无法治疗中枢神经系统中的GAG积累[6],而LEAPER 2.0介导的RNA编辑能够在多个器官中恢复细胞内源IDUA转录本的功能,从而实现了更优的治疗效果。
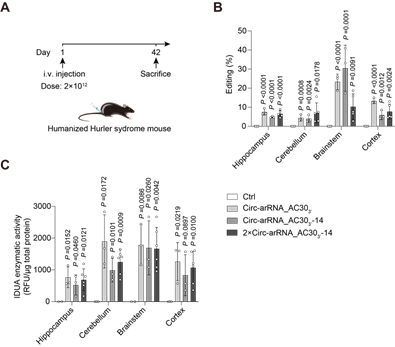
图2. AAV递送的LEAPER 2.0成功治疗人源化Hurler综合征小鼠
结合研究者在非人灵长类动物和人源化小鼠中的研究结果,LEAPER 2.0 为遗传性疾病治疗以及其他严重疾病的潜在临床应用提供了巨大的希望。这些发现极大地加强了通过AAV递送的工程化环状ADAR招募RNA用于治疗和探索性转化研究的前景。这项研究由博雅辑因生物科技有限公司和北京大学魏文胜课题组合作完成。博雅辑因科学创始人,北京大学魏文胜教授和博雅辑因袁鹏飞博士为该研究的共同通讯作者。魏文胜课题组伊宗裔博士、博雅辑因赵艳霞博士、易泽轩博士和张永建博士为论文的共同第一作者,博雅辑因汤刚彬博士等人也对这项研究作出了重要贡献。该研究项目得到了国家重点研发计划、国家自然科学基金重点项目、北京市科委生物医学前沿创新推进项目、北大-清华生命科学联合中心、昌平实验室和中国博士后科学基金的支持。
原文链接:https://genomebiology.biomedcentral.com/articles/10.1186/s13059-023-03086-6
参考文献:
1. Sheridan C: Shoot the messenger: RNA editing is here. Nat Biotechnol 2023, 41(3):306-308.
2. Qu L, Yi Z, Zhu S, Wang C, Cao Z, Zhou Z, Yuan P, Yu Y, Tian F, Liu Z et al: Programmable RNA editing by recruiting endogenous ADAR using engineered RNAs. Nat Biotechnol 2019, 37(9):1059-1069.
3. Yi Z, Qu L, Tang H, Liu Z, Liu Y, Tian F, Wang C, Zhang X, Feng Z, Yu Y et al: Engineered circular ADAR-recruiting RNAs increase the efficiency and fidelity of RNA editing in vitro and in vivo. Nat Biotechnol 2022, 40(6):946-955.
4. Agarwal S: High-dose AAV gene therapy deaths. Nat Biotechnol 2020, 38(8):910.
5. Mort M, Ivanov D, Cooper DN, Chuzhanova NA: A meta-analysis of nonsense mutations causing human genetic disease. Hum Mutat 2008, 29(8):1037-1047.
6. Parini R, Deodato F: Intravenous Enzyme Replacement Therapy in Mucopolysaccharidoses: Clinical Effectiveness and Limitations. Int J Mol Sci 2020, 21(8).