检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
2021年07月13日,北京大学生命科学学院张传茂教授实验室在《美国科学院院刊》(PNAS)(https://www.pnas.org/content/118/28/e2026421118)上长文在线发表题为“Sufu negatively regulates both initiations of centrosome duplication and DNA replication”的研究论文。该项工作发现Sufu独立于其在Hedgehog信号通路中的经典功能,作为一个主控开关(“master switch”),同时负调控中心体和DNA复制起始的分子机制。
中心体是由两个垂直的筒状中心粒和外周基质组成的。中心体复制与DNA复制在每个细胞周期中均仅发生一次并被协同调控,其中中心体复制起始于轮毂样结构的装配,而DNA复制起始于复制前复合体(pre-RC)的装配。许多参与DNA复制的蛋白也在中心体复制过程中发挥功能。然而,中心体复制和DNA复制起始的上游协同调控因子及其调控机制仍有待研究。
该团队在本项工作中发现,敲除Sufu的细胞发生中心体扩增(中心体过度复制)以及多极纺锤体形成,而恢复Sufu表达,能够抑制中心体过度复制,恢复中心体正常数目,并进一步实验证实Sufu负调控中心体的复制。详细研究发现,Sufu通过介导CDK2对CP110的磷酸化修饰负调控中心体复制。
该团队进一步研究发现,敲除Sufu的细胞具有核体积增大、染色体数目变多、胞质分裂异常等表型。提高Sufu在细胞内的蛋白含量,能够减弱核内的pre-RC蛋白与染色体的结合,同时促使它们由核内转运进入胞质,从而抑制DNA复制起始。深入研究表明,Sufu通过增强Skp2、CDK2与Cdt1的结合,促进核内Cdt1的降解,进而负调DNA复制。
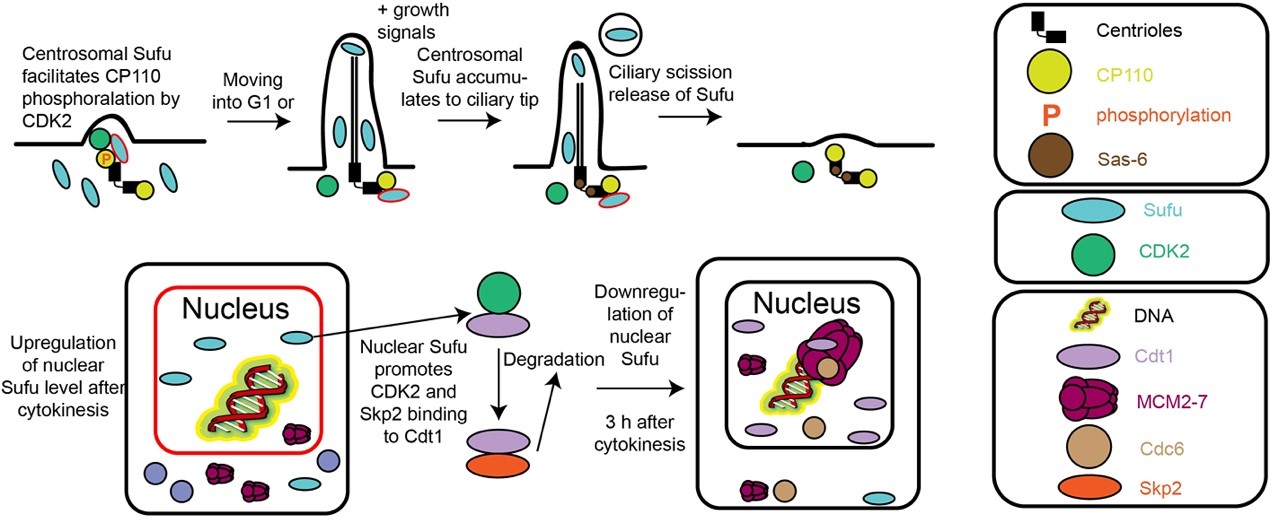
Sufu同时负调控中心体复制和DNA复制起始的分子机制示意图
综上所述,这项工作鉴定出Hedgehog信号通路相关蛋白Sufu是一个中心体复制和DNA复制起始调控的上游调控蛋白,是一个主控开关,并初步揭示了Sufu蛋白调控中心体复制起始和DNA复制起始的分子机制。该项工作为解释细胞周期和中心体周期的协同调控提供了新的理论基础,也为中心体复制和DNA复制各自的调控机制提供了新的视角,有助于进一步探索细胞周期和中心体周期互作失调引起的人类相关疾病的发病机制和治疗靶点。
北京大学生命科学学院张传茂教授为本论文的通讯作者,2014级博士研究生庄腾寒为本论文第一作者,实验室张博言和宋奕泓等其他几位成员以及合作者南京医科大学基础医学院的程雁教授等为该项工作做出了贡献。该项工作受到科技部和国家自然科学基金委项目资助。
实验室介绍
张传茂:
北京大学生命科学学院教授,国家杰出青年基金获得者,国家基金委”创新研究群体“学术带头人,科技部干细胞专项首席,全国优秀科技工作者,全国模范教师,国家自然科学奖二等奖,全国高校科学技术奖一等奖和北京大学拜耳学者奖。
实验室研究领域:
张传茂教授实验室长期以来主要以细胞生物学、分子生物学和生物化学方法技术等为研究手段,以培养细胞,小鼠、非洲爪蟾、果蝇等为主要实验材料,在分子、亚细胞、细胞、组织和个体水平上,从事干细胞增殖与分化、细胞周期调控(包括纺锤体装配和核膜装配机理等)、细胞核结构、细胞核动态变化及功能、Ran GTP酶功能调控、肿瘤细胞增殖调控等方面的研究。