检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
2020年11月24日,北京大学生命科学学院高宁研究组在Cell Discovery杂志发表题为“Structural insight into the assembly and conformational activation of human origin recognition complex”的研究论文,报道了人源DNA复制起始复合物ORC组装过程中两个关键复合物ORC2-5和ORC1-5的冷冻电镜结构,从结构上部分阐释了人源复制起点识别复合物ORC的分步组装和逐步激活的分子机制。
真核生物DNA复制包含有一个复杂的复制起始调控机制,以保证在一个细胞周期内基因组仅复制一次。复制起始的第一步是由ORC(由ORC1-6六个亚基组成)识别并标记DNA复制起始位点,然后招募复制解旋酶,组装成复制体。ORC的功能紊乱与一些人类疾病直接相关,ORC亚基的突变与罕见遗传发育疾病MGS(Meier-Gorlin syndrome)直接相关。MGS患者在胚胎期生长迟缓并伴随多种发育畸形,出生后发育也严重受阻并导致身材矮小、小耳症和膝盖骨缺失等症状。此外,一些致病性DNA病毒(如人类疱疹病毒)需要劫持人源DNA复制系统进行病毒基因组的复制,它们通过招募ORC到病毒DNA复制起点实现这一过程。
在酿酒酵母中,ORC结合到DNA以后,在细胞周期的不同阶段中,始终以六聚体形式稳定结合。2018年,高宁教授与合作者Bik Kwoon Tye教授和翟元樑博士以结构研究为基础,阐释了酿酒酵母ORC特异性识别DNA复制起点的分子机制(Nature, 2018)。人源ORC有着更为复杂的功能调控机制:ORC2-5四个亚基形成一个相对稳定的核心复合物,ORC复合物组装到DNA上依赖于ORC1,ORC1自身的蛋白水平以及ORC1与ORC2-5的结合或解离都受到细胞周期的调控。目前尚不清楚人源ORC复合物分步组装到DNA复制起点的机制。
为了探索人源ORC的组装过程和功能激活机制,高宁组解析了ORC2-5和ORC1-5两种复合物的电镜结构(图1)。ORC2-5结构中,ORC2-WHD结构域插入到ORC与DNA结合的中央孔道内,从而阻挡了DNA的进入,很好地解释了ORC2-5功能自抑制的分子机理。ORC1-5中只有ORC1-WHD稳定结合到了ORC2-5复合物上,ORC1-AAA+尚未完全稳定,存在多种构象状态。一个重要的发现是ORC1-5存在两种主要的结构状态:State I 与ORC2-5的结构大致相同,也处于一种自抑制的构象;在State II中,ORC2-WHD向中央孔道外旋转了120度,部分暴露了位于复合物中央的DNA结合通道,表明State II是一种部分解除抑制效应的构象。这些结果从结构层面上诠释了ORC1在ORC功能激活中的重要角色:ORC1结合到ORC2-5复合物上可以促进ORC2-WHD的构象变化,从抑制状态向激活状态转变,同时ORC1-AAA+结构域保持高度动态,以促进DNA进入ORC的中央通道。
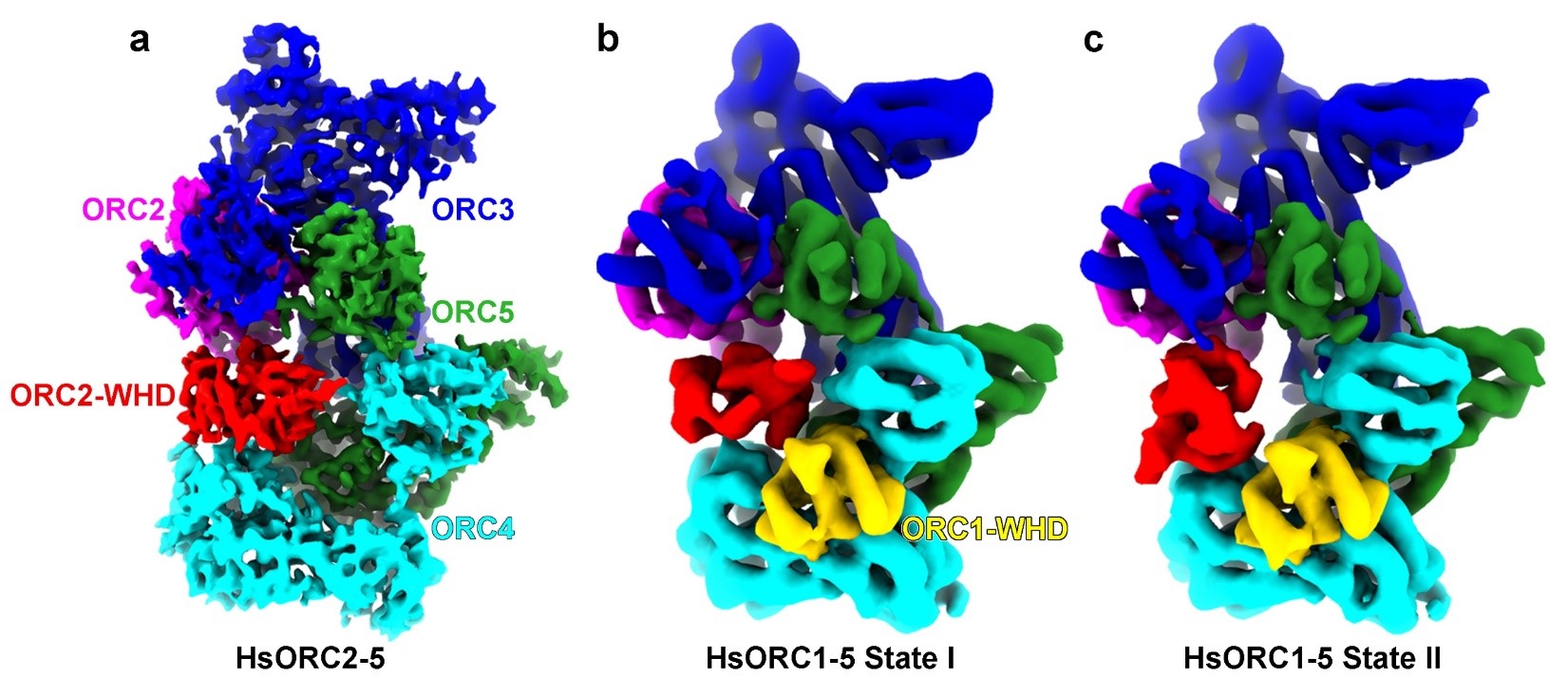
图1,人源ORC2-5和ORC1-5的冷冻电镜结构
结合以往的研究结果,这篇工作进一步完善了人源ORC组装到复制起点的模型(图2):ORC1首先通过特有的BAH结构域结合到携带有特定修饰的核小体上,随后招募ORC2-5核心复合物,形成ORC1-5复合物。通过一系列的构象激活,例如ORC2-WHD结构域的旋转,染色质DNA进入到ORC1-5复合物的中央孔道。伴随着后续的CDC6及ORC6的结合,激活的ORC进一步招募复制解旋酶从而完成Pre-replication complex 的组装。
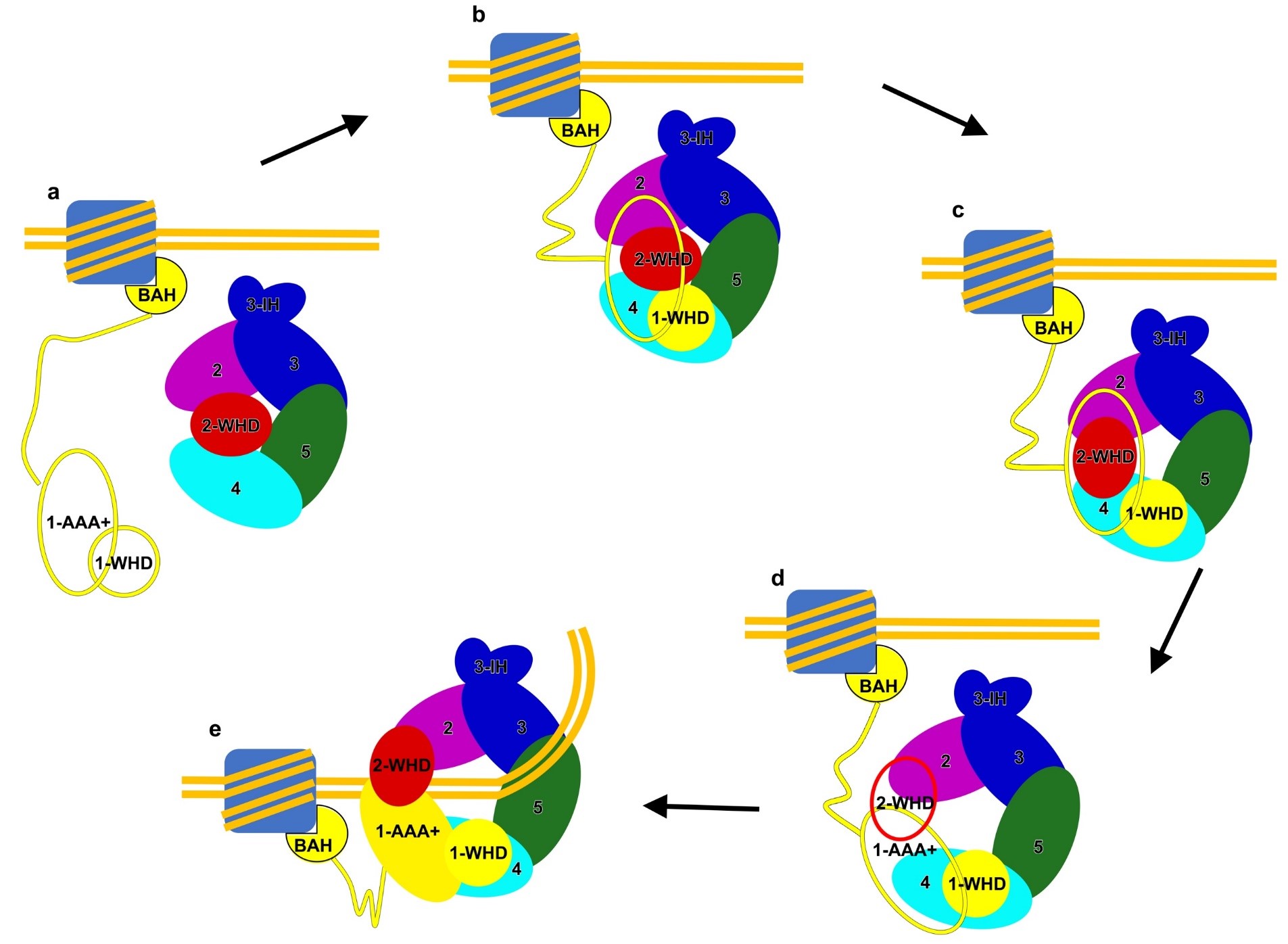
图2,人源ORC逐步组装到复制起点的模型
北京大学生命科学学院、生命科学联合中心高宁教授和高宁组李宁宁副研究员为本文的共同通讯作者。高宁组2016级博士生程稼萱和李宁宁为共同第一作者。香港大学翟元樑研究员和北京大学胡家志研究员为本课题提供了重要的指导与帮助。本课题受到了国家自然科学基金委员会、科技部的项目资助,以及北京大学冷冻电镜平台、电镜实验室、高性能计算平台、生命科学联合中心、生科院仪器中心、膜生物学国家重点实验室的支持。